基于Cytori Cell TherapyTM进行的临床试验项目是由严谨的,精心设计的,对照研究,研究目标为临床上有重要医学需求且现有治疗手段无法满足患者需求的临床适应症。
进行中的临床试验
- 硬皮病
- 骨关节炎
- 运动医学
- 糖尿病足
- 肛瘘
- 烧伤和放射性损伤
- 压力性尿失禁
- 勃起功能障碍
- 研究者启动的研究
- 心脏病
- 急性心肌梗死
- 乳房整形和乳腺癌术后重建
-
硬皮病
硬皮病(Scleroderma)/ 系统性硬化症(Systermic scleroderma)是一种以局限性或弥漫性的皮肤增厚,纤维化为特征,可累及多个内脏器官的自身免疫结缔组织疾病。病因尚不明确,发病初期难确诊,易误诊为类风湿性关节炎,皮肤病,白癜风等。依据其皮肤病变的程度及病变累及的部位,可以分为局限性和系统性两种类型。
硬皮病是一种免疫系统罕见疾病*,具有如下特点:
● 罕见免疫系统疾病
● 影响人群比例,女性: 男性, 4:1
● >90% 的病患存在手部运动障碍
● 纤维化, 疼痛, 水肿及其导致的进一步的手部灵活度和手部基本功能的减弱
2015年4月,欧盟委员会在欧洲药品管理局委员会的推荐下,授予Cytori细胞疗法使用ADRCs注射治疗硬皮病为孤儿药资格。
美国开展的STAR试验,欧洲开展的SCLERADEC I/II试验
STAR(Scleroderma Treatment With Celution Processed Adipose Derived Regenerative Cells)试验是一个在美国20个临床试验机构进行的随机,双盲,安慰剂对照的III期临床试验,入组了80位存在手部功能障碍的硬皮病患者。试验目的是为了评估单次接受Cytori细胞疗法TM治疗的安全性和有效性:硬皮病手部功能障碍的治疗称为HABEOTM。大于90%的硬皮病患者存在手部功能问题,典型表现为手部巨痛,血流量发生异常和功能失常。本研究的初期观察点为Cochin手部功能评分–一种有效测量手部功能的方法。其他的评估观察点为雷诺现象以及其他客观测量手部功能和手指溃疡。完成48周随访期后,安慰剂对照组病人会接受Cytori细胞疗法TM治疗。STAR试验于2016年6月完成全部入组。
STAR试验是基于先前已发表的SCLERADEC I的临床试验结果,该试验在法国马赛大学进行。SCLERADEC I 报道了硬皮病手部功能障碍病人在手部功能,疼痛,雷诺现象方面均有显著改善。SCLERADEC I试验是由Cytoti提供支持的。此外,Cytori支持了正在法国进行的多中心,对照研究SCLERADEC II。
SCLERADEC I试验3年结果表明,硬皮病I期临床实验数据表明,接受治疗的病人在多个观察期均得到持续有效的改善。临床结果指标 基线水平 3年 改善程度(%) P值* 病人报告结果 Cochin手部功能评分(手部功能好0-90手部功能困难) 48.5±10.8 21.3±13.5 56% <0.0001 雷诺现象评分 (无困难0→10 极度困难) 7.2±0.9 0.7±1.6 90% <0.0001 痛感 (VAS/10) 59.4±17.2 26.3±25.9 56% 0.0015 硬皮病健康评估问卷 (无难度0→3 不能动) 1.36±0.3 0.83±0.6 39% 0.005 客观手部功能评价 力气*: 捏力 (kg) 3.3±0.9 4.4±1.8 42% 0.05 力气*: 握力 (kg) 15.4±6.0 18.8±6.8 22% 0.012 伸展度: Max. 食指到拇指的弯曲度(mm) 110.7±24.6 123.5±26.3 12% <0.0001 改善的Rodnan皮肤评分 (手部皮肤厚度) 10.92±4.85 6.25±4.88 43% <0.0001 毛细管显微镜检查 基线水平 12月 血管抑制评分 1.7±0.8 1.1±0.7 35% <0.001 巨大毛细血管数(总数) 41.4±34.1 17.8±22.0 57% 0.0034 分枝毛细血管数 (总数) 45.0±47.9 26.2±22.2 42% 0.110
正在开展的STAR III期试验和SCLERADEC II期试验介绍:试验名称 STAR (Phase III) SCLERADEC II (Phase III)* 研究规模 80 40 随机性 1:1, 治疗组: 对照组 1:1 (治疗剂量数据来自I期结果, 安慰剂) 交叉对照设计 安慰剂, 观察期 48 周 安慰剂, 观察期 24 weeks (包含细胞储存) 试验机构 美国20个硬皮病治疗机构 法国的6个硬皮病治疗机构 主要观察指标 接受治疗6月时Cochin 手部功能评分(CHFS) 接受治疗3月时的Cochin 手部功能评分(CHFS) 次级观察指标 CHFS, 雷诺现象评分, 硬皮病健康评估问卷, 疼痛感, 改善的Rodnan 皮肤评分, 硬皮病测试中的手部活动度, 不良事件 CHFS, 雷诺现象评分, 硬皮病健康评估问卷, 疼痛感, 改善的Rodnan 皮肤评分,毛细管显微镜检查, 不良事件 随访期 48周 24 周 临床试验状态 完成入组, 预计2017年中公布数据 入组中 STAR:是使用Celution分离的脂肪来源再生细胞治疗硬皮病的缩写,英文名称为“Scleroderma Treatment With Celution Processed Adipose Derived Regenerative Cells”,详细信息请参考STAR官网:http://startrial-us.com/。

硬皮病患者治疗6月后,手部愈合情况良好,手部功能显著改善
-
骨关节炎
目前已经完成ACT-OA试验,一个取得美国FDA研究用设备豁免(IDE)的ECCO-50 IIA/B期的临床试验,该试验治疗了94位影响膝盖的骨关节炎患者。该研究在48周随访期的多个时间进行了安全性和有效性指标的评估,评估指标包括症状缓解,功能和活动能力。
-
运动医学
对于职业运动员来说,平均每个赛季受伤2次,且35%的伤情与关节扭伤、韧带损伤、软骨损伤和半月板损伤,而严重的关节损伤可能会毁掉职业运动员的整个赛季。目前,使用Cytori细胞疗法对澳大利亚职业橄榄球运动员的不同类型的运动损伤进行治疗,帮助运动员恢复健康,从而延长了运动员的职业生涯。
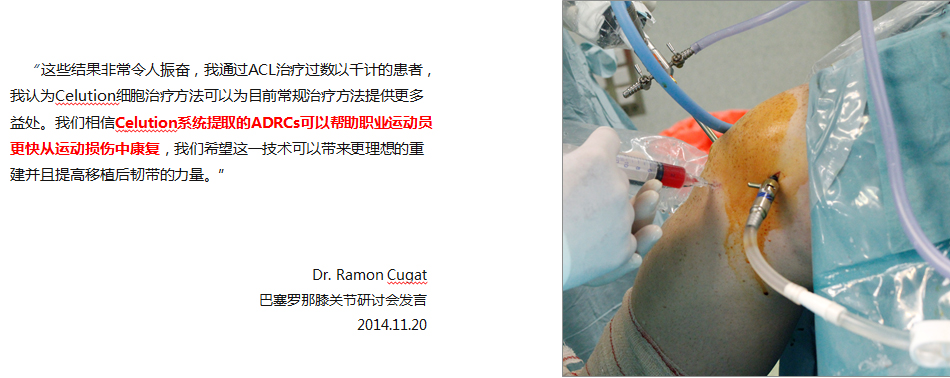
Celution获取ADRCs可以用于膝关节注射治疗通过西班牙卫生部认可

-
糖尿病足
糖尿病足是指由糖尿病引起下肢远端神经异常和外周血管病变有关的足部感染及深层组织破坏。
我国糖尿病患病率逐年升高,现今糖尿病患者已超过1亿,而50岁以上糖尿病人群下肢动脉病变比例为19.47%;我国糖尿病患者1年内新发溃疡发生率为8.1%,糖尿病足溃疡患者1年内新发溃疡发生率为31.6%。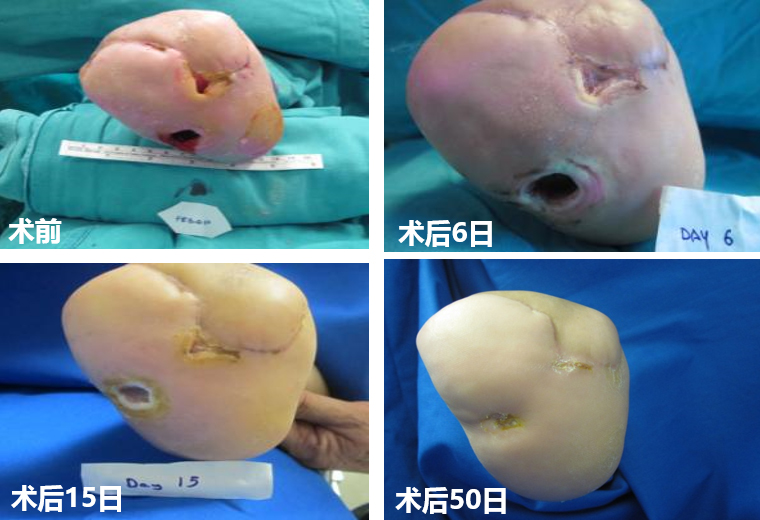
ADRCs治疗糖尿病足,效果显著。
-
肛瘘
肛瘘是指直肠或肛管与肛周皮肤之间形成的瘘管,也称为肛门直肠瘘。瘘管的内口多位于齿状线附近,而外口位于肛周皮肤。瘘管由增厚的纤维组织及肉芽组织组成。
肛瘘一般是肛窦感染形成肛周脓肿并破溃后所形成的,也有无明显脓肿形成而直接发展为肛瘘的。此外,直肠肛门部的创伤、手术、结核、溃疡性结肠炎、克罗恩病等也是肛瘘形成的常见原因。
目前,使用Cytori细胞疗法通过注射ADRCs到瘘管周围,治疗复杂性肛瘘取得显著的效果。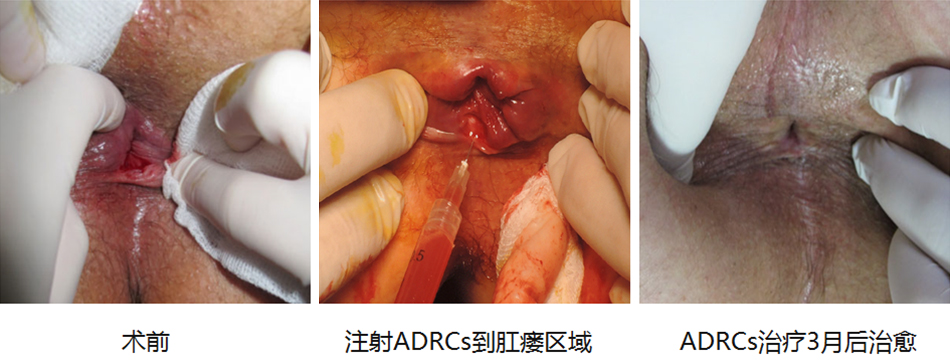
已完成的ADRCs治疗肛瘘的临床试验结果:
序号 国家 医院 治疗疾病 病人数 治疗效果 1 英国 University Hospital of North Tees 肛瘘 7 6月随访结果:5位病人的瘘管闭合;其中一位病人在治疗10月后由于坏血病复发,其余4位病人在随访时间中位数为46个月时痊愈。治疗过程中无任何不良反应和新的尿失禁出现。ADRC富集的脂肪移植用于治疗复杂性肛瘘是安全和有效的。 2 塞尔维亚 Clinical Center of Serbia and at the BelPrime Clinic 肛瘘 6 全部病人肛瘘完全愈合且症状完全消失。疼痛完全停止的平均时间为33.7 ± 15.0天。在手术后3个月,全部病人的肛瘘愈合且移植保持到手术后12个月。整个手术过程没有任何不良反应。 3 日本 Osaka University Graduate School of Medicine 直肠瘘 6 结果表明,瘘管闭合率在术后4周、12周和24周的闭合率分别为83.3%,100%,100%。手术过程中无任何严重不良反应。Celution系统分离的ADRCs细胞数量充足,对于治疗胃肠术后的瘘管是非常有效的。 4 英国 University Hospital North Tees 肛瘘 3 全部病人在2-3年后痊愈 -
烧伤和放射性损伤
2017年4月10日,美国FDA批准了Cytori Cell Therapy治疗烧伤病人的研究用设备豁免(IDE)。已经启动的RELIEF试验是一项前瞻性,非盲,平行组,常对护理对照,多中心,随机的,评估Cytori Cell Therapy作为治疗烧伤病人身体表面20%-50%区域常规护理的补充治疗手段的安全性和有效性。该试验入组了30位病人,治疗组:对照组=2:1,在美国10个临床试验机构开展,观察期为6个月。临床前研究数据表明,Cytori Cell Therapy对多组织烧伤和大剂量放射性损伤有明显疗效。RELIEF试验数据预计于年底公布。
2012年12月,Cytori关于烧烫伤的研究项目获得了美国健康与公共事业部下属的生物医学高级研究与开发机构(BARDA)高达1.06亿美元的资助,2016年9月该资助金额已经提高到1.22亿美元。Cytori Cell Therapy已经作为美国国家层面应对烧伤包括复杂性放射损伤的战略储备技术,同时可以满足烧伤治疗的公共健康需求,而且能够快速和广泛的由非专业医务人员使用。
烧烫伤病人接受ADRCs注射18月后,康复效果显著
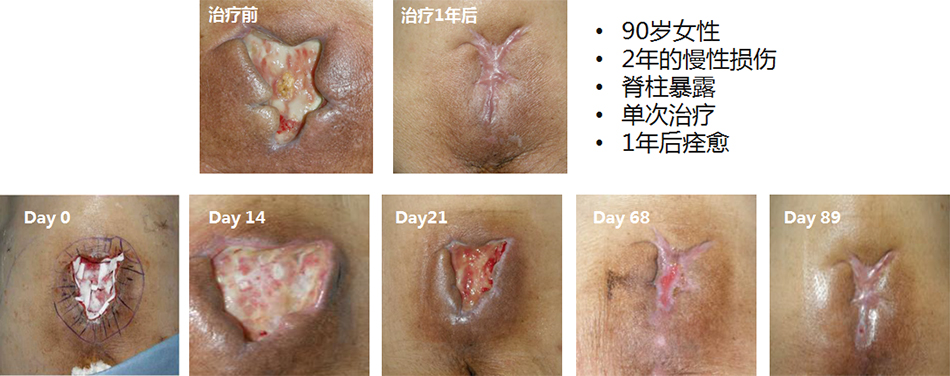
-
压力性尿失禁
Cytori对在日本进行的由研究者和政府共同启动的Cytori Cell Therapy治疗接受前列腺切除手术后的压力性尿失禁临床试验提供了一定支持。此实验是基于之前在名古屋大学进行2项有效性研究试验的结果。试验结果表明,在尿液渗漏,尿道闭合压力和病人生存质量方面年均有明显改善。该试验由日本卫生部,劳动厚生省和名古屋大学共同赞助完成。
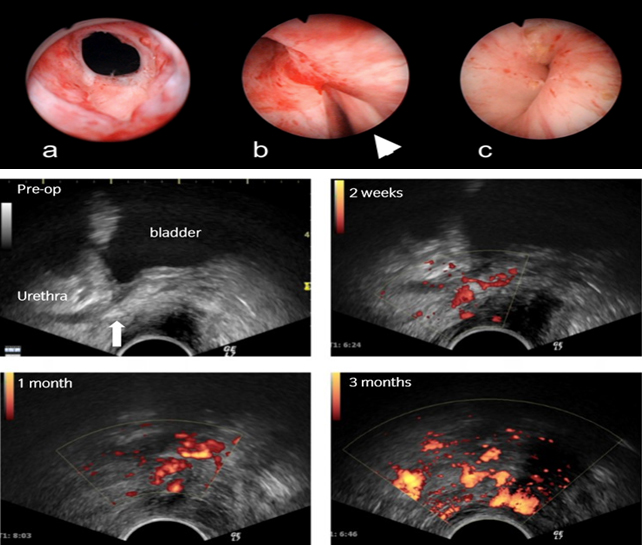
a.术前: 尿道括约肌张开;b.术中:注射ADRCs;c.术后: 尿道括约肌闭合; f~g.ADRCs注射后,尿道周围血液供应显著改善(红色区域)
接受治疗的尿失禁病人,ADRCs注射治疗效果显著
-
勃起功能障碍
勃起功能障碍(ED)是指阴茎持续不能达到和(或)维持足够的勃起以获得满意的性生活(性交)的现象。40%的男性在40岁时会经历不同程度的无法勃起或维持勃起,70岁的男性ED发生率为70%。50%~75%的糖尿病患者会发生勃起功能障碍,ED是糖尿病的第一征象。心血管疾病、动脉粥样硬化、肾脏疾病和多发性硬化患者,往往是通过影响全身的血流或神经冲动引起勃起功能障碍。中国男性,ED患病人口约1.2亿。
已开展的使用Cytori细胞疗法治疗ED的临床试验结果表明,海绵体注射ADRCs治疗ED,效果显著,且安全有效。序号 国家 医院 病人数 治疗效果 1 俄罗斯 Central Clinical Hospital with Outpatient Health Center of Business Administration for the President of Russian Federati 6 治疗6位血管性勃起功能障碍的男性患者,术后6月的观测结果表明:IIEF评分由术前的13±5提高到17.1±5,SEP评分由术前的1.6±0.4提高到3.5±1.8,EHS评分由术前的2±1.4提高到4±0.5,收缩期血流速度超过了30 cm/秒,全部病人在接受治疗后出现了晨勃。 2 丹麦 Odense University Hospital 17 治疗17位前列腺根除术的勃起功能障碍,一年的观察期内,17位患者有8位恢复勃起功能且能完成正常的性交过程。病人的IIEF评分和勃起功能均有显著改善。 -
研究者启动的研究
在获得CE认证和I类认证后,Celution® 系统成为临床医生重要研究工具。这使得他们可以在伦理委员会批准的临床研究中探索Cytori Cell Therapy的临床应用潜力。已经完成一系列的研究人员主导的临床试验,包括一系列的临床疾病治疗应用,如下:
• 前交叉韧带修复(Anterior cruciate ligament repair)
• 骨组织修复(Bone repair)
• 烧烫伤(Burn scar)
• 慢性损伤,慢性溃疡(Chronic wounds)
• 严重肢体缺血(Critical limb ischemia)
• 克罗恩病和直肠阴道瘘(Cryptoglandular and Crohn’s Fistulae)
• 勃起功能障碍(Erectile Dysfunction)
• 半月板修复(Meniscal Repair)
• 压力性尿失禁(Stress urinary incontinence)
• 硬皮病手部功能障碍(Scleroderma hand disease)
• 声带修复(Vocal cord repair) -
心脏病
PRECISE试验是一个在欧洲进行的评估Cytori Cell Therapy在治疗27位慢性心肌缺血的安全性和有效性的临床试验。PRECISE试验的数据表明Cytori Cell Therapy在治疗严重心脏病患者是可行的,该试验为在美国进行的ATHENA试验提供了数据基础。
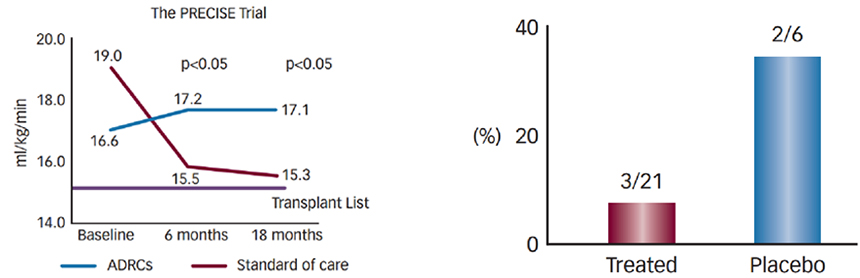
PRECISE
试验结果:接受ADRCs治疗18月后心室功能改善(左图),28月后死亡率降低(右图)。ATHENA I和II试验是多中心,随机,双盲试验,目的是为了评估Cytori Cell Therapy在治疗由缺血性心脏病引起的心脏衰竭的安全和有效性。每个试验均计划入组45位病人和检测两种注射剂量下的治疗。
这两个试验包含多个观察指标,包括6月和12月时氧耗量峰值,灌注缺陷,心力衰竭症状,健康相关的生活质量,左心室收缩末期心舒容积和左心室射血分数。由于试验延迟,注册人数最后减少为31人。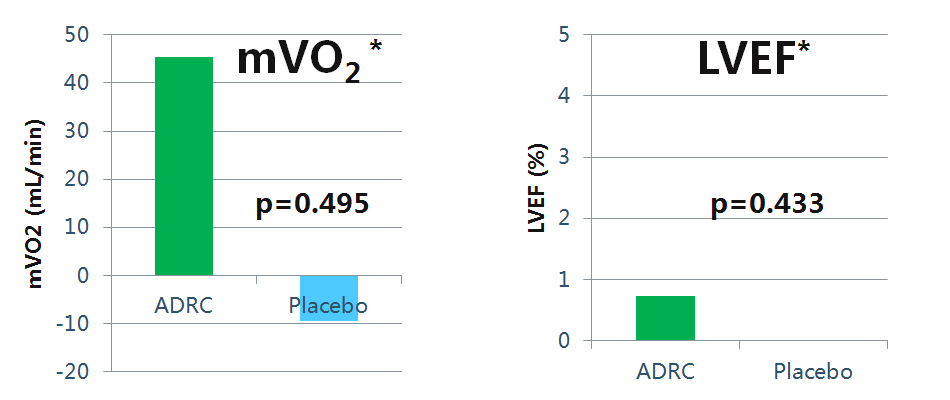
6月观察结果,mVO2和LVEF指标改善,说明心脏生理机能增强
*mVO2Max代表:(1)心室功能(泵血能力) ;(2)血管功能(运氧能力) ; (3)代谢能力(氧气利用能力) ;*左室射血分数,即LVEF(Left Ventricular Ejection Fractions),是指:每搏输出量占心室舒张末期容积量的百分比。正常情况下LVEF≥50%,若小于此值即为心功能不全。
-
急性心肌梗死
APOLLO试验是在欧洲进行的评估Cytori细胞疗法治疗14位ST段抬高型心肌梗死病人的安全性和有效性试验。病人入组和36月随访完成。研究表明,Cytori细胞疗法在治疗ST段抬高型心肌梗死病人进行冠状动脉注射是可行的,也为ADVANCE试验提供了数据支持。
ADVANCE试验是一个入组23位病人,随机,安慰剂对照的,双盲,在欧洲4个中心进行的临床试验。该试验评估Cytori细胞疗法治疗ST段抬高型心肌梗死病人的效果,数据支持现有的Cytori细胞疗法的安全性。
-
乳房整形和乳腺癌术后重建
RESTORE-2研究是一个欧洲IV期(上市后)试验,评估Cytori Cell Therapy在治疗接受部分乳腺切除和放射性治疗后导致的乳房缺陷。这项前瞻性,单臂,开放,多中心临床研究入组了71位病人,缺陷体积范围在25-150mL。整个试验过程表明是安全和无副作用的。数据结果表明,医生和病人的满意率分别为75%和85%。
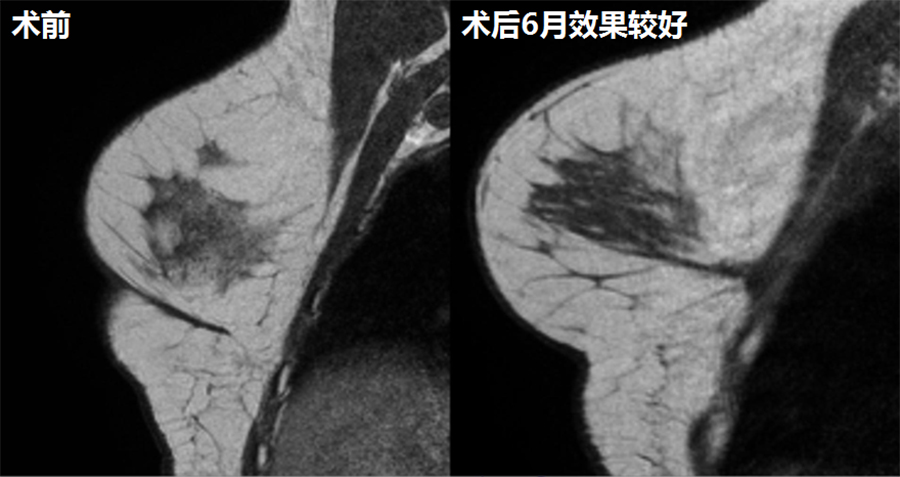 RESTORE-2是一个前瞻性,多中心临床试验,评估ADRC富集的脂肪移植对接受保乳治疗病人的乳房重建效果;研究试验点:西班牙(2),英国(2),比利时(2),意大利(1)
RESTORE-2是一个前瞻性,多中心临床试验,评估ADRC富集的脂肪移植对接受保乳治疗病人的乳房重建效果;研究试验点:西班牙(2),英国(2),比利时(2),意大利(1)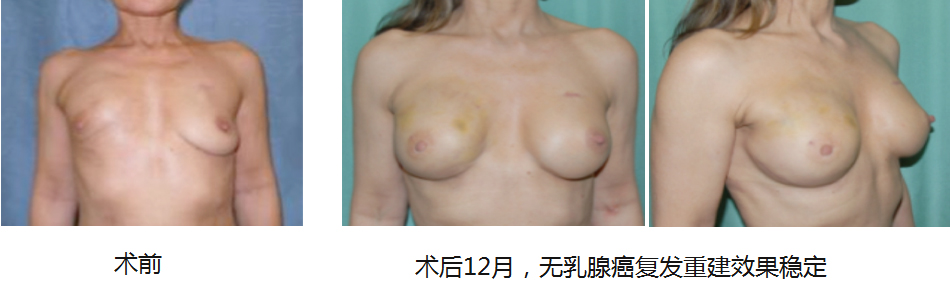
已结束的使用ADRCs进行乳房整形和乳房重建的试验结果汇总:序号 案例(地区) 试验目标 试验结果 1 67(西班牙 ,英国,比利时,意大利) 乳房重建 1年跟踪结果:
核磁共振成像结果(胸型变化): 54 人变大或者明显变大;
医生满意度:75%;
病人满意度:85%;
不良反应:无;2 20(日本) 乳房填充 9 月跟踪结果:
胸围增加 (均值) : 3.3 cm;
医生满意度:69%;
病人满意:75%;
不良反应:无;3 9(意大利) 乳房重建 1年跟踪结果:
胸部皮下厚度:MMQ和 SMQ值均有显著增加;
不良反应:无;4 10(意大利) 乳房重建 1年跟踪结果:
全部病人对胸部结构, 柔和度,胸型和核磁共振结果满意。5 10(日本) 乳腺癌术后修复 跟踪结果:
7.8 ± 1.5年的随访期内,手术过程无严重术后并发症,返回的报告结果对乳房外观和手术整体满意度分别为66.7% 和55.6%。6 21(日本) 乳腺癌术后修复 跟踪结果:
组织厚度测试结果,表明ADRCs 富集的脂肪移植后1月差异显著;随访8月结果,病人满意度为79%。
| 序号 | 临床试验名称 | ClinicalTrials.gov ID |
| 1 | Comparison Between Celution Preparation and Manual Preparation of Adipocyte Derived Regenerative Cells, Using Stromal Vascular Fraction Cell Counts (COMPARE) | NCT01127230 |
| 2 | Effectiveness and Safety of Autologous ADRC for Treatment of Degenerative Damage of Knee Articular Cartilage(膝关节软骨退行性损伤) | NCT02219113 |
| 3 | Effectiveness and Safety of Adipose-Derived Regenerative Cells for Treatment of Erectile Dysfunction(勃起功能障碍) | NCT02472431 |
| 4 | Effectiveness and Safety of Adipose-Derived Regenerative Cells for Treatment of Glaucomatous Neurodegeneration(青光眼神经退行性病变) | NCT02144103 |
| 5 | Effectiveness and Safety of Autologous ADRC for Treatment of Anterior Cruciate Ligament Partial Rupture(前交叉韧带部分断裂) | NCT02469792 |
| 6 | Characterization of Adipose Derived Regenerative Cells (ADRCs) From Patients With Chronic Heart Disease(慢性心脏疾病) | NCT02732106 |
| 7 | Scleroderma(硬皮症) Treatment With Celution Processed Adipose Derived Regenerative Cells (STAR) | NCT02396238 |
| 8 | Celution Prepared Adipose Derived Regenerative Cells in the Treatment of Osteoarthritis of the Knee(膝关节炎) | NCT02326961 |
| 9 | Safety and Efficacy of Adipose Derived Regenerative Cells (ADRCs) Delivered Via the Intracoronary Route in the Treatment of Patients With ST-elevation Acute Myocardial Infarction (AMI)(急性心肌梗塞) | NCT01216995 |
| 10 | SurgiWrapTM to Reduce Soft Tissue Attachment & Incidence Early Post-Operative Bowel Obstruction(肠梗阻) in Colorectal Surgery(结直肠外科手术) | NCT00531739 |
| 11 | A Randomized Clinical Trial of Adipose-derived Stem Cells in Treatment of Non Revascularizable Ischemic Myocardium(心肌局部缺血) | NCT00426868 |
| 12 | Feasibility of Obtaining ADRCs From Discarded Thermal Burn Eschar Tissue(遗弃的热烧伤痂组织) Using Investigational Celution® System | NCT02362386 |
| 13 | Effectiveness and Safety of Autologous Adipose-Derived Regenerative Cells for the Treatment of Urethral Strictures(尿道狭窄) | NCT01889888 |
| 14 | Outcomes After Centrifugation Versus PureGraft for Fatgrafting to the Breast | NCT01979757 |
| 15 | Assessment of the Subcutaneous Reinjection of Human Autologous Adipose-derived Stromal Vascular Fraction (Celution® System) in the Hands of Patients Suffering From Systemic Sclerosis(系统性硬化) | NCT01813279 |
| 16 | Safety & Efficacy of Adipose-Derived Regenerative Cells in the Treatment of Chronic Myocardial Ischemia (ATHENA II)(慢性心肌缺血) | NCT02052427 |
| 17 | Safety and Feasibility Trial of Adipose-Derived Regenerative Cells in the Treatment of Chronic Myocardial Ischemia (慢性心肌缺血) | NCT01556022 |
| 18 | Study of Autologous Fat Enhanced w/ Regenerative Cells Transplanted to Reconstruct Breast Deformities After Lumpectomy(乳房肿瘤切除手术) | NCT00616135 |
| 19 | Randomized Clinical Trial of Adipose-Derived Stem Cells in the Treatment of Pts With ST-elevation Myocardial Infarction(心肌梗塞) | NCT00442806 |
| 20 | Treatment of Breast Cancer Related Lymphedema(乳腺癌相关的淋巴水肿) With Cell-assisted Lipotransfer | NCT02592213 |
| 21 | Effectiveness and Safety of Adipose-Derived Regenerative Cells for the Treatment of Critical Lower Limb Ischemia(重要的下肢缺血) | NCT02864654 |
| 22 | Effectiveness and Safety of Adipose-derived Regenerative Cells for Reduction of Risk of Bladder Neck Contracture(膀胱颈挛缩) | NCT02869061 |
| 23 | Injection Laryngoplasty(喉成型术) Using Autologous Fat Enriched With Adipose Derived Regenerative Stem Cells (ADRC) | NCT02904824 |
| 24 | Clinical Trial of Autologous Adipose Derived Regenerative Cells for the Treatment of Male Stress Urinary Incontinence(男性应激性尿失禁) | NCT02529865 |
| 25 | Effectiveness and Safety of Cell-Assisted Lipotransfer for the Treatment of Stress Urinary Incontinence(压力应激性尿失禁) | NCT01850342 |
| 26 | Assessment of the Efficacy and Tolerance of Sub-cutaneous Re-injection of Autologous Adipose-derived Regenerative Cells in the Local Treatment of Neuropathic Diabetic Foot ulcERs(局部神经性糖尿病足溃疡) | NCT02866565 |
| 27 | Adipose-Derived Regenerative Cells in Total Knee Arthroplasty(全膝关节形成术) | NCT02262988 |
| 28 | STYLE — A Trial of Cell Enriched Adipose For Androgenetic Alopecia(脱发) | NCT02503852 |
| 29 | A Novel Method for Chronic Anal Fissure(肛瘘)Treatment | NCT02628522 |
| 30 | Autologous Stromal Vascular Fraction of Cells for Treatment of Knee Articular Cartilage Dystrophy(膝关节营养不良) | NCT02827851 |

 微信公众平台
微信公众平台